GLPBIO 的小鼠外周血淋巴细胞分离试剂盒(Mouse Peripheral Blood Lymphocyte Separation Kit)是一种基于密度梯度离心原理,简单、快速、高效地从小鼠外周血、脐带血或骨髓细胞中分离出淋巴细胞和单核细胞等细胞的分离试剂盒。

Sample solution is provided at 25 µL, 10mM.
GLPBIO 的小鼠外周血淋巴细胞分离试剂盒(Mouse Peripheral Blood Lymphocyte Separation Kit)是一种基于密度梯度离心原理,简单、快速、高效地从小鼠外周血、脐带血或骨髓细胞中分离出淋巴细胞和单核细胞等细胞的分离试剂盒。本试剂盒主要组分为外周血淋巴细胞分离液,也称为淋巴细胞分离液(Lymphocyte Separation Medium, LSM)、淋巴细胞梯度分离液、Density gradient medium、PBMC分离液、PBMC样本密度分离液或PBMC细胞分离液。本试剂盒中小鼠外周血淋巴细胞分离液与小鼠外周全血近于等渗。本试剂盒中的分离液,和Ficoll-Paque、Ficoll-Hypaque、Histopaque等在使用方法上几乎完全一致。
小鼠外周血细胞包括红细胞(Red blood cell, RBC, 即Erythrocyte)、白细胞(White blood cell, WBC, 即Leukocyte)和血小板(Platelet)。红细胞是血液中数量最多的一类血细胞,是血液运送氧气最主要的媒介,哺乳动物成熟的红细胞是无核的;白细胞是一种不均一的细胞群,生理学上根据其形态、功能和来源分为多核的粒细胞(Granulocyte,包括中性粒细胞、嗜酸性粒细胞和嗜碱性粒细胞)及单核的细胞(Peripheral blood mononuclear cell, PBMC,包括淋巴细胞(Lymphocyte)和单核细胞(Monocyte));血小板是从骨髓成熟的巨核细胞胞浆裂解脱落下来的小块胞质,体积很小,具有凝血、止血功能[1]。
淋巴细胞是体积最小的白细胞,约占白细胞的20-40% [2]。淋巴细胞由淋巴器官产生,主要存在于淋巴管中循环的淋巴液里,是具有特异免疫识别功能的细胞系,在机体抗炎症、抗感染及抗肿瘤等免疫过程中发挥着重要作用[3,4]。根据发生迁移、表面分子和功能的不同,淋巴细胞分为T淋巴细胞、B淋巴细胞和自然杀伤(NK)细胞三大类。其中T淋巴细胞和B淋巴细胞均来自造血组织。T淋巴细胞参与细胞免疫(Cell-mediated immunity),主要免疫功能包括抗胞内感染、抗瘤细胞和异体细胞等。目前有重要临床应用的CAR-T (Chimeric antigen receptor T cell,嵌合抗原受体T细胞)就是一种基于T淋巴细胞的细胞免疫疗法。B淋巴细胞参与体液免疫(Humoral immunity),其主要功能是产生抗体,提呈抗原及分泌细胞因子参与免疫调节;NK细胞由骨髓中的淋巴干细胞分化而来,可直接发挥细胞毒性效应,杀伤病毒感染细胞、肿瘤细胞和异体细胞。淋巴细胞检测是临床血常规项目之一,淋巴细胞异常提示细菌或病毒感染、淋巴细胞系统增殖性疾病、再生贫血障碍等。因此,分离和检测淋巴细胞具有重要临床意义。
人外周血中不同血细胞的体积、形态和比重(密度)有所差异:红细胞和粒细胞的比重较大,约1.092;单核的细胞(淋巴细胞和单核细胞)的比重约为1.075,血小板约为1.030 [5]。因此利用一种分离液,其比重在1.075-1.090之间,淋巴细胞和单核细胞由于比重较小在这种分离液中浮起,而红细胞和粒细胞的比重较大,在该分离液中将下沉,从而将单核的细胞从外周血细胞中分离出来。最常用的分离液是采用聚蔗糖(Polysucrose 400/Ficoll 400)和泛影酸钠(Sodium diatrizoate)配制的混合比重约1.070的溶液[6]。
啮齿类动物的淋巴细胞比重稍高于人淋巴细胞[7-8],本试剂盒提供的小鼠外周血淋巴细胞分离液经过一定的配方优化和改良,和小鼠外周血近于等渗。通过本试剂盒中分离液及配套的PBMC高效离心管(5ml)进行密度梯度离心,离心管中的细胞或液体由上至下分四层:血浆和血小板密度较低,悬浮于分离液的上部,为第一层;单核的细胞(PBMC,包含淋巴细胞和单核细胞)的密度稍低于分离液,位于分离液界面之上,一般为环状乳白色,为第二层,所以移去第一层就可获得PBMC;第三层为透明分离液层;红细胞与粒细胞密度较大,沉于底部,为第四层。
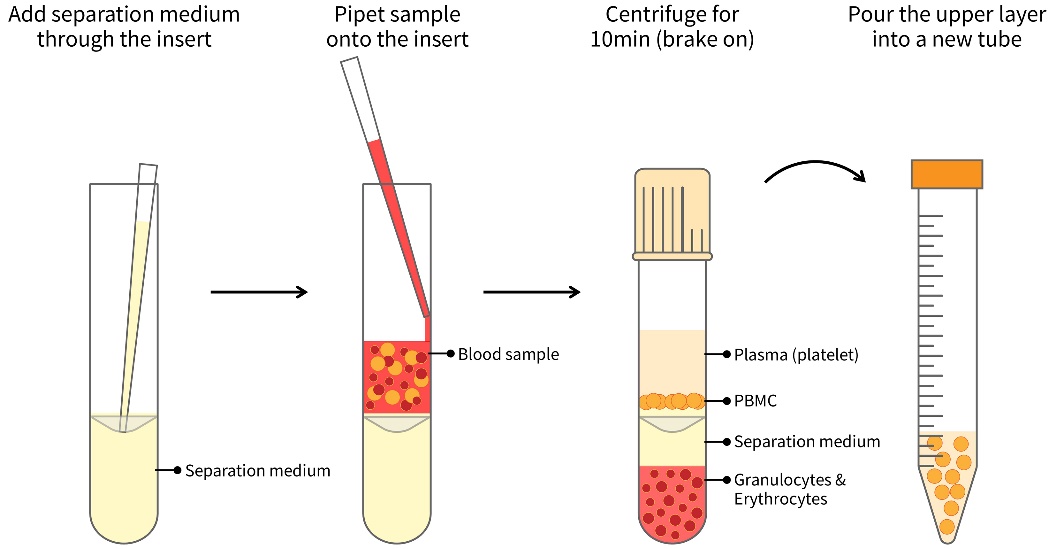
图1. 小鼠外周血淋巴细胞分离试剂盒分离小鼠外周血效果示意图。
本试剂盒标配PBMC高效离心管(5ml),内置独特的分离嵌套(Insert)设计 ,可最大程度减少样品和分离液的混合,无需费时费力的进行繁琐且需细心的分层操作,既可以减少人为操作对实验结果造成的影响,又可以便捷、高效分离获得PBMC。
本试剂盒操作简单,操作时间短,分离率高。整个实验只需要简单的移液、离心操作,即可在约15分钟内完成样品淋巴细胞的分离。本试剂盒对于淋巴细胞分离的提取率大于80%。如需获得高纯度目的细胞,可配合使用免疫磁珠进行分选。使用本试剂盒预分离,可减少磁珠的使用量,降低成本。
本试剂盒品质高,质量控制严格。本试剂盒中分离液使用药用级原料,配方经过优化处理,无菌,内毒素小于0.5EU/ml。
本试剂盒应用范围广。本试剂盒不仅适用于稀释后的抗凝血液样品,也可用于未经稀释的抗凝血液样品;可分离淋巴细胞,还可分离一定纯度的血浆;分离得到的淋巴细胞可直接检测,也可进行细胞培养。
按使用说明操作,样品体积为2ml时,200ml本试剂盒可进行约100次淋巴细胞分离。
保存条件:
室温保存,两年有效。本试剂盒严禁冷藏或冷冻保存。其中小鼠外周血淋巴细胞分离液须避光保存。
注意事项:
本试剂盒可能不适合部分C57小鼠外周血淋巴细胞的分离,因为可能会出现红细胞沉降不完全或完全不沉降的现象。
小鼠外周血淋巴细胞分离液使用本前须颠倒混匀,并在无菌条件下吸取,避免微生物污染。
如果要对分离的淋巴细胞进一步培养,须在收集血液和分离过程中,注意无菌操作,避免微生物污染。
本试剂盒宜室温保存,严禁冷藏冷冻保存。低温条件下,小鼠外周血淋巴细胞分离液会出现白色结晶,影响分离效果。
由于小鼠外周血淋巴细胞分离液在低温时密度升高,而在高温的时候密度会降低,因此使用本试剂盒的温度要求是18-22ºC,最佳分离温度是20ºC。不同血液样品,分离效果不同。离体时间较长、运输等因素可能导致其分离效果不佳。血液样品宿主的身体状况、使用药物情况、患病情况及性别等因素均可能影响分离效果。
部分塑料的离心管(如聚苯乙烯, PS)带有静电,可能会导致细胞挂壁,影响分离效果。推荐使用GLPBIO 聚丙烯材质的离心管或无菌硅化离心管,更推荐标配的PBMC高效离心管(5ml),使用更便捷,如需更多,可以单独订购PBMC高效离心管。
PBMC高效离心管(5ml)直径约12mm,高约75mm(不含盖)或83mm(含真空管盖),对于常规的15ml离心机转子,离心时须使用配套的15ml转5ml转子适配器。
当样品体积为0.2-2ml时,建议使用5ml的PBMC高效离心管;当样品体积为0.5-6ml时,建议使用15ml的PBMC分离管;当样品体积为5-25ml时,建议使用50ml的PBMC分离管。
为避免细胞活性降低和提高淋巴细胞分离效果,请选用不含有钙镁离子的缓冲液或生理盐水对血液样品进行稀释。
由于不同种属动物免疫细胞密度的差异,本产品仅适用于小鼠外周血淋巴细胞分离,不适用于其它动物。不同动物血液须选用特定的分离液。
本产品仅限于专业人员的科学研究用,不得用于临床诊断或治疗,不得用于食品或药品,不得存放于普通住宅内。
为了您的安全和健康,请穿实验服并戴一次性手套操作。
使用说明:
1.实验前准备:
a.需自备水平转子离心机(离心力≥1200×g)。整个梯度离心要求是慢升慢降,需要设置离心机的加速度为1-3,关闭刹车,须自然停止。如果使用本试剂盒配套的5ml的PBMC高效离心管,则无须关闭刹车。
b.抗凝剂的选择:若分离出的淋巴细胞直接用于检测,可选用枸橼酸钠抗凝剂;若分离出的淋巴细胞需进一步培养,则选用肝素抗凝剂。
c.血液样品应是新鲜抗凝血,避免冷藏或冷冻。血液样品离体2小时内分离效果最佳;血液样品离体2-4小时,分离效果尚可;血液样品离体4小时以上,分离效果差或无法进行分离操作。
d.为保证最佳分离效果,整个实验过程要求检测样品、使用试剂、离心及实验室的温度均保持在20±2ºC。
2.血液样品的稀释(选做):
a.可使用不含有钙镁离子缓冲液或生理盐水或培养基对样品进行稀释。推荐选择GLPBIO 生产的PBS和生理盐水。
b.按照血液样品:PBS或生理盐水=2:1的比例对血液样品进行稀释。
3.淋巴细胞的分离(当使用5mlPBMC高效离心管时 ):
a.加入分离液。取出分离液并平衡至室温,用移液管吸取约1.8ml分离液从PBMC高效离心管分离嵌套的中心孔内加入,分离液须适量没过分离嵌套上方(above the insert)。
b.保持分离管垂直,用移液器吸取待分离的样品沿着管壁缓慢加入到分离管中。样品将与没过嵌套上方的分离液混合。
注:也可直接将样品倾倒进管内,但须避免样品经嵌套的中央小孔直接进入分离液中。
c.室温450×g离心20-30分钟,无须关闭离心机刹车。离心后,液体分离为4层,从上到下依次为血浆层(含血小板)、乳白色环状层(即PBMC层,包括淋巴细胞(Lymphocyte)和单核细胞(Monocyte))、分离液层和沉淀层(红细胞和粒细胞)(图1)。离心后须小心取出离心管,切勿摇晃或震动。血浆层和乳白色环状层在嵌套上方,统称为上层溶液。
注1:对于常规的15ml离心机转子,离心时须使用相应的适配器。推荐水平转子。
注2:若样品放置超过24小时,则建议适当延长离心时间,可将红细胞分离的更好。
注3:不同品牌和型号的离心机在打开刹车时的减速效果可能不同。如果离心后看不到PBMC层或者PBMC的回收率较低,可将刹车速率降低至中或低。
注4:如有必要,可以通过增加离心时间、降低离心力进行离心。
d.将含PBMC层的上层溶液倒入另一干净的普通离心管中。离心管推荐BeyoGold™ 15毫升锥形离心管。
注1:分离管中的分离嵌套可避免PBMC被红细胞和粒细胞再次污染,但分离管倒置时间不要超过2秒。
注2:收集或吸除PBMC所在层以上5-10mm的血浆层,可防止富集的细胞被血小板再次污染。
注3:离心后,分离管中分离嵌套的表面可能存在一些红细胞 ,这些红细胞不会影响分离效果。
e.加入适量稀释液(5-10ml PBS或HBSS),适当混匀,重悬细胞。室温300×g离心8分钟,弃上清。重复洗涤2次。
f.所得沉淀即为分离的淋巴细胞,用适量PBS或合适的培养液将收集到的PBMC重悬备用。
4.淋巴细胞的分离(当使用普通离心管时):
a.分离液和血液样品的加入:取一支新15ml无菌离心管或无10ml菌硅化离心管(需自备),先加入一定量分离液;随后将管子小心地倾斜45度,并沿着壁管缓慢地加入血液样品,使样品顺着管壁缓慢滑动到接近分离液液面处,避免血液样品冲入液面下,此时血液样品平铺在分离液的液面上,注意保持两液面界面清晰,切勿搅动液面或摇晃、混匀。
注1:可以使用无菌巴氏吸管吸取血液样品或后续的血浆层、淋巴细胞。
注2:由于分离液和血液的密度差异,将形成明显的分层界面。如果样品较多导致加样时间较长,在离心前出现红细胞成团下沉属正常现象。
b.当样品体积在0.5-2.0ml范围时,使用10ml无菌硅化离心管,先加入4ml分离液,然后加入血液样品,按步骤4c进行离心操作;当样品体积在2.0-4.0ml范围时,使用15ml无菌离心管,先加入5ml分离液,然后加入血液样品,按步骤4d进行离心操作。
注1:可将血液样品和分离液置于20ºC水浴中孵育20分钟,以保证最佳分离温度。
注2:分离液体积不得少于3ml,血液样品不得少于0.5ml。
注3:如使用15ml无菌离心管,血液样品和分离液量总和不得超过10ml。
注4:请根据血液样本量确定离心条件,血液样品量越多,所需离心力越大,所需离心时间越长,具体离心条件需自行摸索,以达到最佳分离效果。
c.对于0.5-2.0ml血液样品量,推荐最佳离心条件为20ºC,450×g,离心30分钟。
d.对于2.0-4.0ml血液样品量,推荐最佳离心条件为20ºC,500×g,离心30分钟。
e.条件的优化:
(1)根据离心后乳白色环状层(淋巴细胞层)显现状态,调整样品稀释倍数。乳白色环状层弥散,应适当提高样品的稀释倍数;乳白色环状层很浅或没有,应适当降低样品的稀释倍数。
(2)根据离心后淋巴细胞存在的分层位置,可适当调整离心力。离心后淋巴细胞在血浆层,适当提高离心力;离心后淋巴细胞在分离液层,则适当降低离心力。
(3)若出现红细胞沉降不完全的情况,可以适当加大离心力。
(4)若出现血小板污染的情况,可适当降低离心力,同时分离后可增加洗涤次数。
(5)离心力的调整以50-100×g为基数,直至达到最佳分离效果。离心力最小不可小于400×g,最大不可大于1200×g。离心时间以20-30分钟为准。
(6)地域差异、四季温差及离心机性能差异等均会影响分离效果,可根据实际情况,调整离心条件。建议对离心条件进行调整时,恒定离心时间,对离心转速进行调整。
f.血浆层的吸取:小心、缓慢地吸取血浆层并转移到新的离心管中,勿触动PBMC层,可留少量血浆层。血浆层样品后续可用于血浆相关检测。如需获得纯度较高的血浆,建议仅吸取血浆层由上至下的2/3的血浆,剩余1/3血浆可能包含部分PBMC及少量分离液成分。离心后的分离效果示意图请参考图1,由上到下分为四层,依次为血浆层(含血小板)、乳白色环状层(即PBMC层)、透明分离液层和红细胞/粒细胞层。离心后须小心取出离心管,切勿摇晃或震动。
g.淋巴细胞的吸取:可直接穿过血浆层,小心、缓慢地吸取乳白色环状层(即PBMC层)并转移到新的离心管中(此方法技术要求高),也可以在尽量吸除血浆层后再小心、缓慢地吸取乳白色环状层,并转移到新的离心管中。
注1:为避免吸取存在分离液交界处的粒细胞,请不要过多吸取淋巴细胞层。
注2:若吸取的淋巴细胞层混杂有红细胞,可使用红细胞裂解液将红细胞裂解,以去除红细胞,提高淋巴细胞分离率。
h.洗涤I:加入10mlPBS或HBSS ,适当混匀,重悬细胞。250×g离心10分钟,弃上清。
i.洗涤II:加入5mlPBS或HBSS,适当混匀,重悬细胞。250×g离心10分钟,弃上清。重复本步骤2-3次。
j.所得沉淀即为分离的淋巴细胞,用适量PBS或合适的培养液将收集到的PBMC重悬备用
| Item | Component | Quantity |
| GC27543-1 | Mouse Peripheral Blood Lymphocyte Separation Medium | 200ml |
| GC27543-2 | PBMC High-Efficiency Centrifuge Tubes (5ml) | 10×2 |
| GC27543-3 | 15ml to 5ml Rotor Adapter | 2 |